Introducción
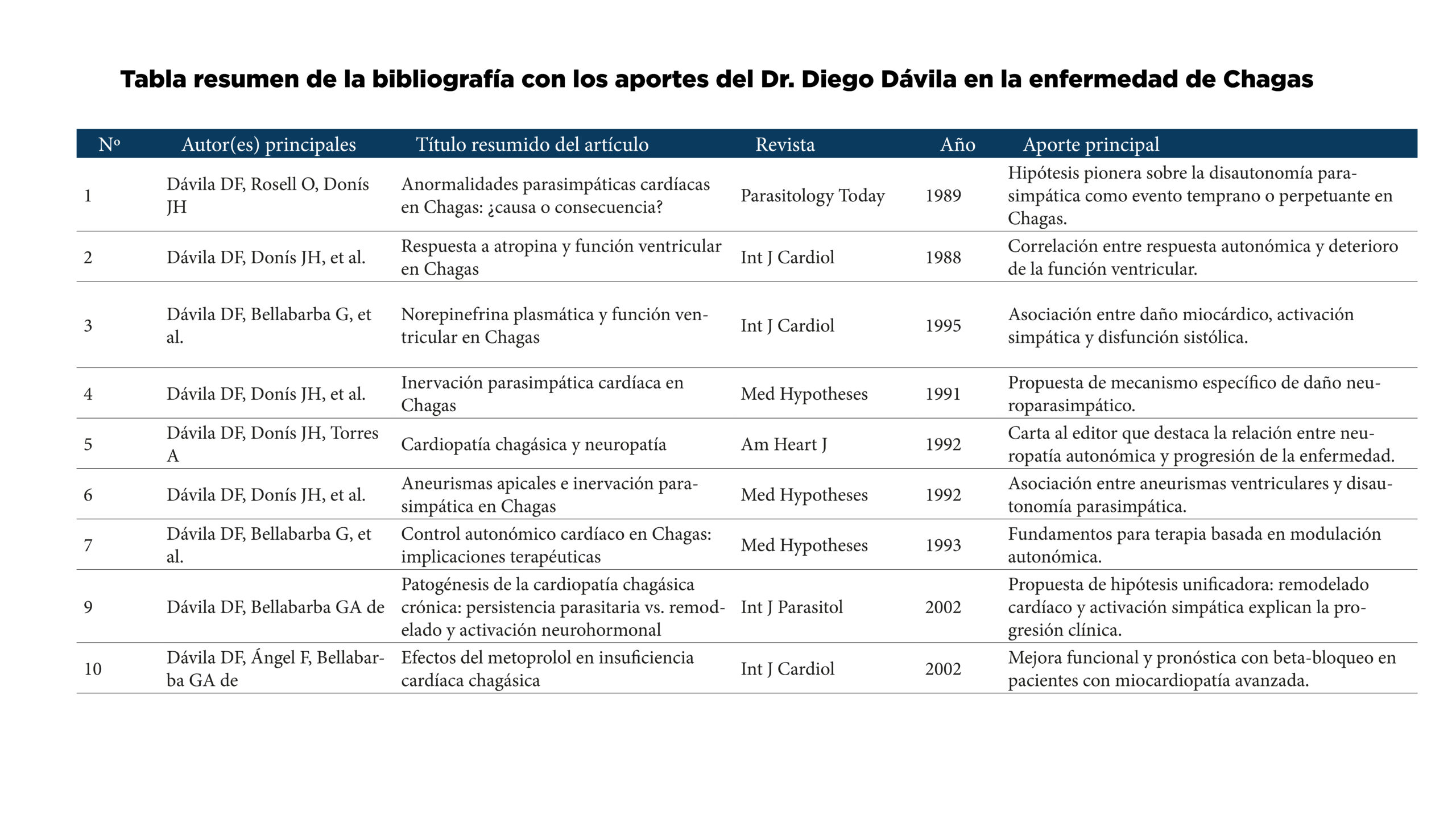
La enfermedad de Chagas, causada por el Trypanosoma cruzi, ha sido históricamente interpretada bajo dos grandes ejes explicativos: la persistencia del parásito en el miocardio y la activación autoinmune del sistema inmunológico. Sin embargo, el Dr. Diego F. Dávila (†), cardiólogo e investigador venezolano, propuso a inicios del siglo XXI un modelo alternativo y complementario: una hipótesis neurogénica unificada, que integra el daño neuronal, la remodelación cardíaca y la activación neurohormonal en el desarrollo progresivo de la miocardiopatía chagásica crónica (1).
Más allá del parásito: límites de las hipótesis tradicionales
Si bien la persistencia parasitaria y las respuestas autoinmunes han sido consideradas causas primarias del daño miocárdico en la fase crónica (2,3), Dávila señala que no explican completamente el espectro clínico de la enfermedad. Muchos pacientes con presencia de T. cruzi en biopsias miocárdicas permanecen asintomáticos durante décadas (fase indeterminada), mientras que otros desarrollan arritmias severas o insuficiencia cardíaca terminal con pobre pronóstico, a pesar de recibir tratamiento antiparasitario (4,5).
La hipótesis neurogénica: una nueva lectura de la progresión
El Dr. Diego Dávila planteó que, durante la fase aguda, el parásito provoca un daño irreversible sobre el sistema nervioso autónomo cardíaco, especialmente las neuronas parasimpáticas. Este desequilibrio deja sin freno al sistema simpático, generando una activación adrenérgica tóxica y sostenida, que inicia un proceso insidioso de daño miocárdico progresivo (6). Sin embargo, esta activación neurohormonal no es precoz: aparece tardíamente, cuando el corazón ya está remodelado y dilatado (1,7).
Remodelado cardíaco y activación neurohormonal
Como en otras miocardiopatías dilatadas (8,9), cuando el daño miocárdico segmentario alcanza un umbral crítico (~20% del tejido), el corazón inicia un proceso de remodelado ventricular. Este proceso implica dilatación progresiva, disfunción contráctil y activación de ejes neurohormonales como el sistema renina-angiotensina-aldosterona y el sistema simpático, lo que produce una espiral de toxicidad por catecolaminas, pérdida de miocitos y sobrecarga hemodinámica (10). Esta progresión es clínicamente silenciosa durante años, hasta desencadenar síntomas graves y eventos letales.
Una propuesta integradora: hipótesis neurogénica modificada
La hipótesis unificada del Dr. Diego Dávila propuso que los pacientes que sufren daño segmentario crítico en la fase aguda tienen más riesgo de progresar a fases avanzadas por mecanismos de remodelado estructural y activación neurohormonal tardía. Esta evolución ocurre en tres fases consecutivas:
- Indeterminada: sin síntomas ni remodelado significativo.
- Arrítmica: aparición de alteraciones electrocardiográficas.
- Congestiva: disfunción ventricular, síntomas severos y mala sobrevida (1,5,11).
Este modelo explica por qué los antagonistas neurohormonales (como betabloqueantes o IECA) mejoran la evolución, incluso sin afectar directamente al parásito (12,13). Así, se plantea que el prognóstico está más ligado al daño funcional y estructural del corazón que a la presencia persistente del parásito en la fase crónica.
Conclusión
La propuesta fisiopatogénica del Dr. Diego Dávila ofrece un enfoque clínico y terapéutico novedoso. Más allá del debate entre parasito-persistencia versus autoinmunidad, su modelo integra la neurofisiología cardíaca, el remodelado ventricular y la activación neurohormonal para explicar la progresión y diversidad fenotípica de la enfermedad de Chagas crónica. Esta visión ha abierto nuevas puertas para la comprensión clínica, el pronóstico y el abordaje terapéutico de esta enfermedad endémica latinoamericana.
Hoy se conmemoran 10 años del fallecimiento del Dr. Diego F. Dávila (†), maestro de generaciones, cardiólogo clínico e investigador insigne del Instituto de Investigaciones Cardiovasculares de la Universidad de Los Andes. Su obra pionera en la comprensión de la disfunción autonómica, el remodelado cardíaco y la neuroactivación simpática en la cardiopatía chagásica constituye un legado invaluable para la medicina latinoamericana. A una década de su partida, su pensamiento científico sigue inspirando nuevas hipótesis, guías terapéuticas y compromisos académicos en la lucha contra esta enfermedad endémica y desatendida.
Referencias
- Dávila DF, Rossell O, Arata de Bellabarba G. Pathogenesis of chronic Chagas heart disease: parasite persistence and autoimmune responses versus cardiac remodelling and neurohormonal activation. Int J Parasitol. 2002;32(1):107–9.
- Tarleton RL. Parasite persistence in the aetiology of Chagas disease. Int J Parasitol. 2001;31(5–6):550–4.
- León JS, Engman DM. Autoimmunity in Chagas heart disease. Int J Parasitol. 2001;31(5–6):554–60.
- Añéz N, Carrasco HA, Parada H, et al. Myocardial parasite persistence in chronic chagasic patients. Am J Trop Med Hyg. 1999;60:726–32.
- Carrasco HA, Parada H, Guerrero L, et al. Prognostic implications of clinical, electrocardiographic and hemodynamic findings in chronic Chagas’ disease. Int J Cardiol. 1994;43:27–38.
- Koberle F. Pathogenesis of Chagas’ disease. In: Ciba Foundation Symposium 20. Amsterdam: Elsevier; 1974. p.137–52.
- Dávila DF, Donís JH, Torres A, Gottberg CF, Rossell O. Cardiac parasympathetic innervations in Chagas’ heart disease. Med Hypotheses. 1991;35:80–4.
- Mann DL. Mechanisms and models in heart failure: A combinatorial approach. Circulation. 1999;100:999–1008.
- Douglas PS, Morrow R, Ioli A, Reichek N. Left ventricular shape, afterload and survival in idiopathic dilated cardiomyopathy. J Am Coll Cardiol. 1989;13:311–5.
- Bristow MR. Beta-adrenergic receptor blockade in chronic heart failure. Circulation. 2000;101:558–69.
- Patel AR, Lima C, Parro A, et al. Echocardiographic analysis of regional and global left ventricular shape in Chagas cardiomyopathy. Am J Cardiol. 1998;82:197–202.
- Szajnnbok FF, et al. Beneficial effects of enalapril on the diastolic ventricular function in Chagas myocardiopathy. Arq Bras Cardiol. 1993;60:273–8.
- Dávila DF, Ángel F, Bellabarba GA de. Effects of metoprolol in Chagasic patients with severe congestive heart failure. Int J Cardiol. 2002;85:255–60.